Dissenyen el primer fotofàrmac per al tractament del dolor
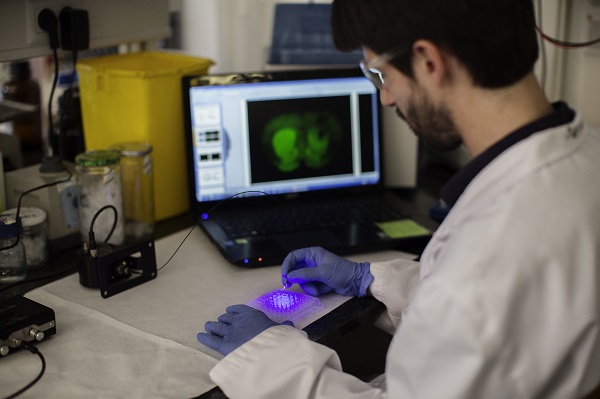
Un equip de lʼInstitut de Neurociències de la Universitat de Barcelona ha participat en el disseny del primer fotofàrmac —el JF-NP-26, activat per la llum— per al tractament del dolor. La recerca, feta amb models animals i publicada a la revista eLife, lʼhan encapçalat els equips dirigits pel professor Francisco Ciruela, de la Facultat de Medicina i Ciències de la Salut de la Universitat de Barcelona, lʼInstitut de Neurociències de la UB i lʼInstitut dʼInvestigació Biomèdica de Bellvitge (IDIBELL), i el Dr. Amadeu Llebaria, del Grup de Química Mèdica i Síntesi (MCS) de lʼInstitut de Química Avançada de Catalunya (IQAC-CSIC).

Un equip de lʼInstitut de Neurociències de la Universitat de Barcelona ha participat en el disseny del primer fotofàrmac —el JF-NP-26, activat per la llum— per al tractament del dolor. La recerca, feta amb models animals i publicada a la revista eLife, lʼhan encapçalat els equips dirigits pel professor Francisco Ciruela, de la Facultat de Medicina i Ciències de la Salut de la Universitat de Barcelona, lʼInstitut de Neurociències de la UB i lʼInstitut dʼInvestigació Biomèdica de Bellvitge (IDIBELL), i el Dr. Amadeu Llebaria, del Grup de Química Mèdica i Síntesi (MCS) de lʼInstitut de Química Avançada de Catalunya (IQAC-CSIC).
Optofarmacologia: fàrmacs que sʼactiven amb la llum
En general, la farmacologia convencional presenta limitacions importants —distribució lenta i imprecisa del fàrmac, falta dʼespecificitat espacial o temporal en lʼorganisme, dificultat en lʼajust de la dosi, etc.— que poden restringir lʼacció terapèutica de qualsevol fàrmac. En aquest context, lʼoptofarmacologia és una disciplina emergent en farmacologia que es basa en lʼús de la llum per controlar lʼactivitat dels medicaments. Així doncs, aplicant llum sobre un fàrmac fotosensible, seʼn pot controlar el procés dʼacció farmacològica amb precisió espacial i temporal.
El nou treball publicat a la revista eLife ha culminat amb el disseny dʼun fotofàrmac (JF-NP-26) amb potencials aplicacions terapèutiques per tractar el dolor, una molècula que es pot activar amb llum localment i quan es vol, és a dir, amb una alta resolució espaciotemporal.
«En lʼàmbit clínic no existeix cap precedent de lʼús de lʼoptofarmacologia per millorar el tractament del dolor ni de cap patologia relacionada amb el sistema nerviós. En el terreny preclínic, és a dir, amb models animals, aquest és el primer fotofàrmac dissenyat per al tractament del dolor in vivo», detalla el professor Francisco Ciruela.
Dissenyant un compost fotosensible sense efectes tòxics
En aquesta nova proposta dʼoptofarmacologia, un fàrmac amb un mecanisme dʼacció conegut (per exemple, un analgèsic) es modifica químicament per fer-lo fotosensible i inactiu. Aquest fotofàrmac sʼactiva quan és irradiat per un feix de llum, dirigit mitjançant una fibra òptica, dʼuna longitud dʼona apropiada i amb precisió mil·limètrica sobre el teixit diana (cervell, pell, articulacions, etc.).
El fotofàrmac JF-NP-26 és el que sʼanomena un photocaged, és a dir, una molècula emmascarada químicament i inactiva, que sʼactiva mitjançant la llum. Comparat amb altres compostos fotosensibles, el JF-NP-26 és una molècula que quan sʼadministra a un animal no té cap efecte farmacològic fins que el teixit diana és irradiat amb llum de lʼespectre visible (amb una longitud dʼona de 405 nm). A més, JF-NP-26 no mostra efectes tòxics ni indesitjables en animals, ni tan sols en dosis elevades en estudis de curta durada.
La il·luminació del fotofàrmac indueix un trencament en la molècula JF-NP-26 que allibera la molècula activa (raseglurant), que bloqueja el receptor metabotròpic de glutamat tipus 5 (mGlu5), implicat en moltes funcions neuronals com ara la transmissió neuronal del dolor. El bloqueig dʼaquest receptor permet anul·lar la transmissió del dolor des de la perifèria del cos fins al cervell de lʼorganisme. Aquest bloqueig el podem produir tant en les neurones perifèriques com en el sistema nerviós central (cervell) i generar, en tots dos casos, un efecte analgèsic com a resultat final.
Un efecte analgèsic poc descrit fins ara
«La molècula generada per lʼacció de la llum —el raseglurant— no pertany a cap grup de fàrmacs de lʼarsenal farmacològic clàssic contra el dolor: els antiinflamatoris no esteroidals o AINE (paracetamol, ibuprofèn) i els opioides (morfina, fentanil). En conseqüència, en aquest treball es descriu un mecanisme analgèsic poc explorat fins ara», detalla el professor Ciruela.
«Curiosament —afegeix lʼinvestigador—, el raseglurant va ser explorat en assajos clínics com a analgèsic contra la migranya però es va descartar per la seva hepatotoxicitat. Aquesta nova aproximació optofarmacològica del raseglurant pot evitar-ne els efectes adversos en el fetge i obre el camí per emprar-lo com a analgèsic».
A la recerca de nous fàrmacs mitjançant lʼoptofarmacologia
Lʼoptofarmacologia perfila un nou horitzó en la descoberta de nous analgèsics i de vies dʼadministració i control de lʼacció farmacològica. Aquesta disciplina pot ajudar a ampliar el ventall terapèutic en la lluita contra el dolor i reduir notòriament els efectes indesitjables de molts fàrmacs (per exemple, el risc elevat dʼaddicció de la morfina, la baixa eficàcia analgèsica dels AINE davant el dolor intens i crònic, etc.).
«Si comparem les molècules biològiques naturals que actuen en els éssers vius amb els fàrmacs, veiem que les primeres funcionen amb una gran precisió, actuant de manera localitzada, amb unes dosis regulades i una durada definida. En canvi, els fàrmacs que tenim actuen a tots els llocs i poc controladament. Lʼús de molècules regulades per llum intenta superar aquestes mancances per poder obtenir fàrmacs més precisos que actuïn imitant les molècules biològiques», afirma el Dr. Llebaria. Lʼequip del Grup MCS de lʼIQAC-CSIC participa actualment en diversos projectes de fotofarmacologia, en concret, en el disseny i la síntesi de diverses molècules activables mitjançant la llum. «Aquesta aproximació és més complexa que la dʼun fàrmac convencional ja que, a més de les propietats terapèutiques, sʼhan dʼoptimitzar les respostes fotoquímiques i fotofísiques de la molècula», apunta Llebaria.
Lʼequip de la UB i lʼIDIBELL està desplegant línies de recerca en optofarmacologia per donar resposta a molts problemes associats a la farmacologia convencional. «En lʼactualitat, estem explorant altres molècules amb mecanismes dʼacció diferent però basats també en receptors de membrana acoblats a la proteïna G, la major diana terapèutica a dia dʼavui. Així doncs, tenim fotofàrmacs que estem estudiant per tractar la malaltia de Parkinson o la psoriasi. També explorem la utilització optofarmacològica de llum amb diferents longitud dʼona (verda, groga i vermella), que són menys tòxiques encara. En un escenari de futur, no podem descartar que algunes simptomatologies es puguin alleujar amb la implantació de fibres òptiques al cervell, tal com sʼimplanten elèctrodes en lʼestimulació cerebral profunda en la malaltia de Parkinson», remarca Francisco Ciruela.
A més dels grups de la UB-IDIBELL i del CSIC, també participen en el treball investigadors de lʼInstitut Químic de Sarrià, la Universitat Autònoma de Barcelona, lʼInstitut de Genòmica Funcional (IGF) de la Universitat de Montpeller (França), la Universitat la Sapienza de Roma i lʼInstitut Neuromed (Itàlia). «Cal destacar la necessitat dʼimpulsar la col·laboració entre grups de recerca de diferents àmbits de la ciència per explorar nous camins que permetin entendre la complexitat biològica i desplegar tot el potencial per crear tecnologies radicalment noves en la millora de la salut humana», expliquen els investigadors que han liderat el projecte.