Descobert un mecanisme de reclutament de cèl·lules assistents en el càncer de pulmó més freqüent
Un equip dʼexperts de la Universitat de Barcelona, la Universitat de Saragossa i lʼHospital Clínic de Barcelona han descobert un mecanisme de reclutament de cèl·lules assistents (anomenades CAF o fibroblasts associats a càncer). És una descoberta científica molt rellevant, ja que les cèl·lules assistents són essencials en lʼadenocarcinoma pulmonar (el tipus de càncer de pulmó més freqüent), atès que contribueixen a totes les fases del desenvolupament tumoral, inclosa la metàstasi.

Un equip dʼexperts de la Universitat de Barcelona, la Universitat de Saragossa i lʼHospital Clínic de Barcelona han descobert un mecanisme de reclutament de cèl·lules assistents (anomenades CAF o fibroblasts associats a càncer). És una descoberta científica molt rellevant, ja que les cèl·lules assistents són essencials en lʼadenocarcinoma pulmonar (el tipus de càncer de pulmó més freqüent), atès que contribueixen a totes les fases del desenvolupament tumoral, inclosa la metàstasi.
En el treball, publicat a la revista British Journal of Cancer, lʼequip també revela que hi ha un tipus de fàrmacs inhibidors que podrien ser útils contra la capacitat migratòria dʼaquestes cèl·lules assistents, de manera que podrien evitar-ne el reclutament i, per tant, la seva posterior contribució al desenvolupament tumoral.
«La importància dʼaquestes dues troballes rau en el fet que lʼadenocarcinoma de pulmó suposa el 40 % dels casos de càncer de pulmó i produeix una metàstasi molt primerenca, fet que afecta directament les possibilitats dels pacients de sobreviure», explica el professor Jordi Alcaraz, coordinador del treball i membre de la Facultat de Medicina i Ciències de la Salut de la UB i lʼInstitut de Bioenginyeria de Catalunya (IBEC). Actualment, la probabilitat de supervivència a cinc anys dʼun càncer de pulmó que no sʼha estès a altres òrgans és superior al 60 %. Ara bé, quan ha arribat a altres parts del cos, les probabilitats es redueixen per sota del 10 %.
Com afecta la proteïna SMAD3 al procés tumoral?
El professor Jordi Alcaraz (UB-IBEC) havia descobert en estudis previs que, en els pacients amb adenocarcinoma, la proteïna SMAD3 està sobreactivada selectivament. Ara, el nou treball examina els efectes de la proteïna SMAD3 en el reclutament de les cèl·lules assistents, i nʼanalitza el potencial impacte en la disseminació del tumor i la generació de metàstasi.
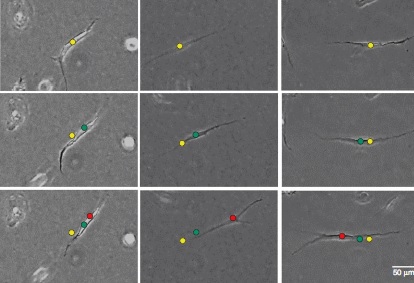
Per això, lʼequip del catedràtic José Manuel García Aznar, de lʼInstitut de Recerca en Enginyeria dʼAragó de la UZ, en què participen els investigadors Yago Juste Lanas i Carlos Borau, va aplicar una tecnologia innovadora basada en dispositius de microfluídica amb matrius extracel·lulars de col·lagen en 3D per estudiar les protrusions de les cèl·lules assistents i la migració cel·lular en ambients que simulen diferents etapes del desenvolupament del tumor.
Les cèl·lules assistents van mostrar un avantatge migratori —un moviment més ràpid i direccional, amb formes més allargades— en un ambient propi dels estadis inicials del tumor. Així mateix, en aquestes cèl·lules assistents es va observar una capacitat proliferativa menor, fet que implicava lʼefecte promigratori de la proteïna SMAD3 com a factor essencial per al reclutament i lʼacumulació de cèl·lules assistents CAF en adenocarcinomes. Com que aquestes cèl·lules assistents contribueixen a totes les fases del desenvolupament tumoral —inclosa la disseminació—, aquesta troballa podria ser decisiva per comprendre la disseminació primerenca de lʼadenocarcinoma a altres òrgans. A més, aquest avantatge migratori es va veure eliminat pel fàrmac inhibidor Trametinib, ja aprovat per tractar altres tipus de tumors, fet que encoratja lʼús terapèutic dʼaquest tipus de fàrmacs en lʼadenocarcinoma de pulmó.
Tal com explica lʼexpert Yago Juste Lanas, membre del grup M2BE de la UZ i primer autor del treball, han descobert que «les cèl·lules assistents dels tumors dʼadenocarcinoma tenen una alta capacitat migratòria». «Això permet que siguin reclutades al tumor més fàcilment, i podria afavorir la formació primerenca de metàstasi, un procés que sʼobserva en els pacients però del qual encara es desconeixen les causes —apunta—. A més, els inhibidors com el Trametinib, segons els nostres resultats, podrien ser efectius contra el reclutament».
En ambients propers a un tumor més desenvolupat, sʼha constatat també que les cèl·lules assistents dʼadenocarcinomes poden establir interaccions més estretes amb les cèl·lules tumorals, a causa de la reducció de la capacitat migratòria observada en aquest estudi. «Ara continuem treballant per entendre si les cèl·lules assistents dʼadenocarcinoma de pulmó també poden afavorir, per altres mecanismes, la disseminació dʼaquests tumors, amb lʼobjectiu últim de poder frenar-ne la metàstasi», explica lʼinvestigador.
Recerca col·laborativa multidisciplinària
Per a lʼèxit de la recerca, un projecte col·laboratiu multidisciplinari, ha estat decisiva la participació de metges, biotecnòlegs, físics i enginyers, principalment. En concret, lʼHospital Clínic de Barcelona va proporcionar les biòpsies de pacients, que els equips de la UB van emprar per obtenir cèl·lules assistents i poder estudiar-ne les alteracions moleculars, com en el cas de la proteïna SMAD3. Per la seva banda, els equips de la UZ han estudiat el moviment dʼaquest tipus cel·lular en entorns fisiopatològics similars als trobats en estadis inicials o tardans del desenvolupament tumoral.
El treball també està signat per Carlos Borau (UZ); Natalia Díaz-Valdivia i Alejandro Llorente (UB-IBEC); Rafael Ikemori, Alejandro Bernardo i Marselina Arshakyan (UB); Josep Ramírez (Hospital Clínic); José Carlos Ruffinelli i Ernest Nadal (ICO-IDIBELL), i Noemí Reguart (Hospital Clínic-IDIBAPS).
Article de referència:
Juste-Lanas, Y., Díaz-Valdivia, N.; Llorente, A. et al. «3D collagen migration patterns reveal a SMAD3-dependent and TGF-β1-independent mechanism of recruitment for tumour-associated fibroblasts in lung adenocarcinoma». British Journal of Cancer, desembre de 2022. Doi: 10.1038/s41416-022-02093-x